Programa Nacional de Control de Salmonella en Gallinas Reproductoras 2025-2027 (Versión 2026): Resumen Práctico
Antecedentes y contexto: de dónde venimos
Este programa no es un capricho nacional; emana del Reglamento (CE) nº 2160/2003 y busca cumplir con los objetivos de la Unión Europea. El objetivo en España sigue siendo claro: reducir la prevalencia de los 5 serotipos «top» a un máximo del 1% en manadas de más de 250 aves adultas.
La vigilancia en España lleva activa desde 1993, pero la presión sobre la bioseguridad y la trazabilidad nunca ha sido tan alta como en esta versión 2026.
Los 5 magníficos: serotipos objetivo
El programa va a la caza y captura de cinco serotipos específicos. Si aparecen estos, tenemos problemas:
- S. Enteritidis
- S. Typhimurium (incluyendo la variante monofásica 1,4,[5],12:i:-)
- S. Infantis
- S. Virchow
- S. Hadar
Dato vital: Una manada se considera positiva no solo si se aísla la bacteria. Si se detectan antimicrobianos o inhibidores de crecimiento bacteriano, la manada se da por positiva automáticamente a efectos del objetivo de la UE. Así que mucho cuidado con los tratamientos.
¿De donde partimos?
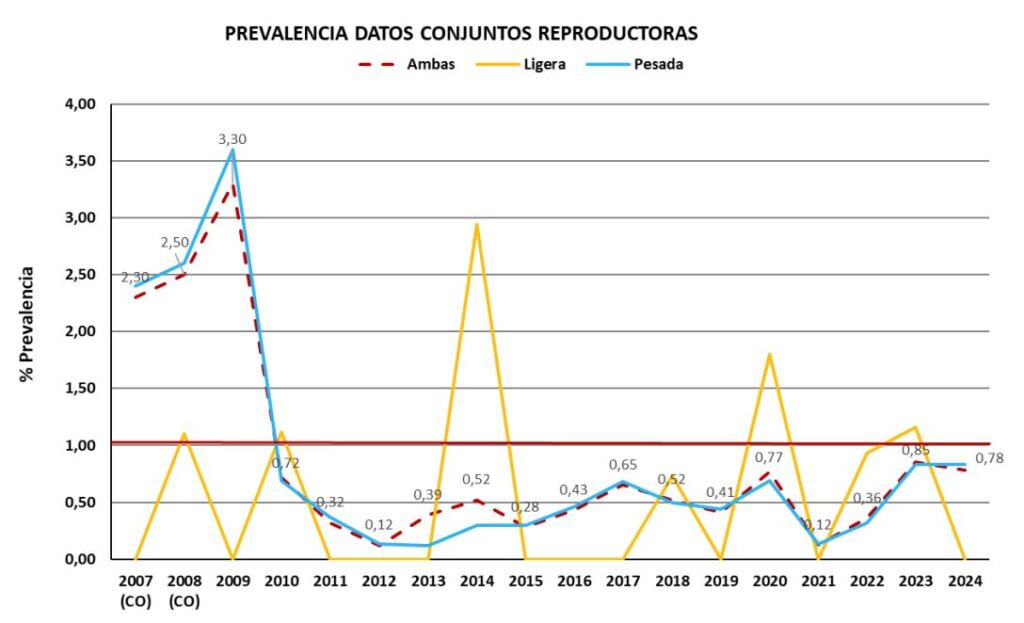
En 2004, España realizó un estudio de referencia en manadas de aves reproductoras Gallus gallus, que reveló una prevalencia del 16,6% frente a los 5 serotipos objetivo y del 20,3% frente a Salmonella spp. en general. A partir de ese dato de partida, se han venido ejecutando programas nacionales sucesivos que han logrado reducir drásticamente la prevalencia hasta situarla, en 2024, en el 0,78%, cumpliendo sobradamente el objetivo comunitario del 1%.
El programa actual cubre el trienio 2025-2027 y esta versión, publicada en febrero de 2026, incorpora las actualizaciones correspondientes al año 2026. Es elaborado y coordinado por la Subdirección General de Sanidad e Higiene Animal y Trazabilidad del Ministerio de Agricultura, Pesca y Alimentación (MAPA), y ejecutado por las Comunidades Autónomas en todo el territorio español.
1. Objetivo del Programa
Controlar y reducir la presencia de 5 serotipos de Salmonella en manadas de gallinas reproductoras Gallus gallus, manteniendo la prevalencia por debajo del 1% en manadas con más de 250 aves adultas.
Serotipos objetivo:
- Salmonella Enteritidis (SE)
- Salmonella Typhimurium (ST), incluyendo la variante monofásica (fórmula antigénica 1,4,[5],12:i:-)
- Salmonella Infantis (SI)
- Salmonella Virchow (SV)
- Salmonella Hadar (SH)
2. Ámbito de aplicación
| Aspecto | Detalle |
|---|---|
| Territorio | Todo el Reino de España |
| Especies | Gallinas reproductoras de la especie Gallus gallus |
| Fases | Reproductoras adultas y recría de reproductoras |
| Explotaciones cubiertas | Todas las autorizadas y registradas por las autoridades competentes |
| Exclusiones | Explotaciones que producen productos primarios destinados al autoconsumo (uso doméstico privado) |
Unidad epidemiológica: la manada, definida como todas las aves con el mismo estatus sanitario que comparten las mismas instalaciones o cubicación de aire.
Identificación de manadas: código REGA + letra de la nave (mayúscula) + fecha de entrada de las aves (formato mmaaaa).

3. Definición de caso positivo
Una manada reproductora se considera positiva cuando:
- Se detecta la presencia de alguno de los 5 serotipos objetivo (distintos de cepas vacunales) en una o más muestras, o
- Se detectan antimicrobianos o inhibidores de crecimiento bacteriano en la manada.
Regla del recuento único: una manada positiva se contabiliza una sola vez por período de producción, independientemente de la frecuencia de detección.
«El objetivo sigue firme:
menos del 1% de prevalencia
en manadas adultas para los 5 serotipos
clave de Salmonella.»
4. Notificación obligatoria
- Toda persona física o jurídica (especialmente los veterinarios) debe notificar los casos confirmados o sospechosos de Salmonella.
- La comunicación a la autoridad competente debe realizarse dentro de las 24 horas siguientes a conocerse los resultados.
- Es obligatorio grabar todos los resultados de autocontroles en la aplicación informática del MAPA.
- Los laboratorios deben serotipar al menos para distinguir entre los 5 serotipos objetivo y otros serotipos.
5. Frecuencia de muestreo
5.1. Autocontroles (a cargo del operador)
| Fase | Momento del muestreo |
|---|---|
| Manadas de cría — Pollitas de 1 día | Al recibir las pollitas en la explotación |
| Manadas de cría — 4 semanas | A las 4 semanas de edad |
| Manadas de cría — Pretrasferencia | 2 semanas antes de entrar en fase de puesta |
| Reproductoras adultas | Cada 2 semanas durante la fase de puesta (ampliable a 3 semanas si se ha cumplido el objetivo comunitario durante 2 años consecutivos) |
Además: muestreo ambiental de verificación tras cada limpieza y desinfección de nave.
5.2. Controles oficiales (a cargo de la autoridad competente)
| Control | Momento |
|---|---|
| 1.er control oficial | Dentro de las 4 semanas posteriores al traslado a la unidad de puesta |
| 2.º control oficial | Durante el periodo productivo, suficientemente alejado de los otros dos |
| 3.er control oficial | Hacia el final de la fase de puesta (no antes de las 8 semanas previas al fin del ciclo) |
Si se ha alcanzado el objetivo comunitario durante 2 años consecutivos, la autoridad competente puede reducir a 2 controles oficiales por ciclo de producción (la mayoría de las CCAA aplican esta excepción).

6. Tipos de muestras y protocolo de muestreo
6.1. Pollitas de un día (recría)
Se puede optar por una de estas tres alternativas:
- Opción 1: Muestra de los revestimientos internos (fondos de caja) de 10 cajas de transporte.
- Opción 2: Hígado, ciego y vitelo de 60 pollitas (procesadas como una sola muestra).
- Opción 3: Meconio de al menos 250 pollitas.
6.2. Aves de 4 semanas y pretransferencia (recría)
Dos opciones:
- Heces frescas: porciones de ≥1 g, recogidas en un mínimo de 10 puntos del local, mezcladas en 2 muestras compuestas como mínimo. El número de porciones depende del censo:
| N.º de aves en el local | Porciones de heces a recoger |
|---|---|
| 1-24 | Igual al n.º de aves (máximo 20) |
| 25-29 | 20 |
| 30-39 | 25 |
| 40-49 | 30 |
| 50-59 | 35 |
| 60-89 | 40 |
| 90-199 | 50 |
| 200-499 | 55 |
| 500 o más | 60 |
- Calzas absorbentes: 5 pares, procesados en laboratorio como 2 muestras compuestas de 5 calzas cada una.
6.3. Reproductoras adultas (autocontrol y control oficial)
Dos opciones:
- Heces frescas (≥1 g cada porción, recogidas al azar), en un mínimo de 2 muestras compuestas:
| N.º de aves de la manada | N.º de porciones de heces |
|---|---|
| 250-349 | 200 |
| 350-449 | 220 |
| 450-799 | 250 |
| 800-999 | 260 |
| 1.000 o más | 300 |
- Calzas absorbentes: 5 pares, procesados como 2 muestras compuestas de 5 calzas.
6.4. Instrucciones específicas por sistema de producción
- Manadas en jaula: heces mezcladas de forma natural procedentes de cintas de recogida, rasquetas o fosos. Mínimo 2 muestras de ≥150 g cada una.
- Jaulas sin acumulación suficiente de heces: 4 o más paños de tela (superficie mínima de 900 cm² por cara), humedecidos, pasados por el final de todas las cintas accesibles.
- Naves de varios niveles o cría en suelo (camperas, ecológicas): 1 par de calzas por zonas de yacija + al menos 2 paños de tela humedecidos por cintas recolectoras de estiércol.
«En recría, el muestreo no perdona:
día 1,
semana 4
y dos semanas antes del traslado.
Sin excepciones.»
7. Método analítico
- Norma de referencia: EN/ISO 6579-1 (modificación 1 — EN/ISO 6579-2017/Amd1:2020).
- Medio de enriquecimiento: medio semisólido Rappaport-Vassiliadis modificado (MSRV), incubado a 41,5 ±1 °C durante 2 × (24 ±3) horas.
- Serotipado: conforme al esquema de Kaufmann-White-Le Minor, al menos 1 cepa por muestra positiva.
- Métodos alternativos: admitidos si están validados según EN ISO 16140 y registrados en el MAPA.
- Plazos máximos para serotipado:
| Etapa | Plazo máximo |
|---|---|
| Envío de aislado a otro laboratorio | 24 h tras el aislamiento |
| Inicio del serotipado en el laboratorio receptor | 24 h tras la recepción |
| Emisión y envío del informe de resultados | 24 h tras obtener el resultado |
8. Transporte y conservación de muestras
- Las muestras deben enviarse al laboratorio en las 24 horas posteriores a su recogida (preferiblemente por correo urgente o mensajería).
- Si no se envían en 24 h, deben almacenarse refrigeradas.
- Transporte a temperatura ambiente aceptable si se evita calor excesivo (>25 °C) y exposición solar directa.
- En laboratorio: mantener refrigeradas; examen dentro de 48 h tras recepción y 96 h tras el muestreo.

9. Medidas de bioseguridad
Las medidas de bioseguridad se verifican mediante un protocolo de verificación con puntuación por áreas. Los elementos evaluados incluyen 15 bloques temáticos, con requisitos excluyentes (marcados con **) que invalidan la puntuación si no se cumplen:
| Bloque | Puntuación máx. | Aspectos clave |
|---|---|---|
| 1. Control de acceso a la explotación | 9-12 puntos | Vallado perimetral, desinfección de vehículos, registro de visitas, pediluvios |
| 2. Mantenimiento de instalaciones | 5 puntos | Plan de mantenimiento, limpieza de entorno, estanqueidad de naves |
| 3. Control del agua de bebida | 2 puntos | Procedencia (red municipal o análisis periódicos), depósitos protegidos |
| 4. Gestión de estiércoles y residuos | Excluyente | Plan de gestión aprobado y registrado |
| 5. Gestión de cadáveres y SANDACH | 4 puntos | Sistema de eliminación, contenedores cerrados, recogida desde fuera del vallado |
| 6. Control de acceso de personal | 9 puntos | Pediluvios en naves, vestuarios con zona limpia/sucia, ropa exclusiva |
| 7. Abastecimiento de pollitas | 3 puntos | Carga/descarga exterior, registros, documentos sanitarios, certificados |
| 8. Control de piensos | 13 puntos | Proveedores autorizados, almacenamiento correcto, certificados de análisis |
| 9. Limpieza, desinfección y desinsectación (LDD) | 12 puntos | Programa documentado, análisis de eficacia, vacío sanitario ≥12 días (o ≥7 con prueba de eficacia) |
| 10. Control de roedores y otros animales | 11-13 puntos | Plan de desratización documentado, sin animales domésticos en zona de producción |
| 11. Control de medicamentos veterinarios | 2 puntos | Libro de registro de medicamentos, almacenamiento seguro |
| 12. Supervisión veterinaria | 1 punto | Veterinario responsable con visitas y controles registrados |
| 13. Prácticas de manejo y formación | 6 puntos | Código de Buenas Prácticas, sistema todo dentro/todo fuera, formación de operarios |
| 14. Programa sanitario de huevos incubables | 13 puntos | Programa de recogida, clasificación y sanitización documentado |
| 15. Autocontroles | Excluyente | Cumplimiento de frecuencias de muestreo en recría y producción |

10. Medidas ante una manada positiva
10.1. Si se detecta alguno de los 5 serotipos objetivo
- Investigación epidemiológica rigurosa para identificar la fuente de infección.
- Inmovilización: prohibición de movimiento de aves vivas (salvo autorización para sacrificio o destrucción, con documento sanitario oficial).
- Sacrificio o destrucción de todas las aves de la manada (incluidos pollitos de un día).
- Huevos no incubados: se destruyen (o se destinan a consumo humano solo si se garantiza la destrucción de Salmonella).
- Huevos en incubadora: se destruyen o tratan conforme al Reglamento (CE) 1069/2009.
- Refuerzo de bioseguridad en todas las manadas de la explotación.
- Limpieza y desinfección completa de la nave (incluida retirada total de yacija y excrementos), seguida de desinsectación y desratización.
- Prohibición de repoblación durante los 12 días posteriores a la desinfección (reducible a 7 días si los análisis ambientales demuestran eficacia).
- Comunicación de todas las fechas clave a la autoridad competente.
- Reproductoras pesadas: además de todo lo anterior, el siguiente lote debe entrar vacunado frente a Salmonella.
- Control de trabajadores: posibilidad de solicitar análisis laboratoriales del personal.
10.2. Si se detecta un serotipo no objetivo
- Investigación epidemiológica (especialmente si son resultados recurrentes).
- Refuerzo de bioseguridad en todas las manadas de la explotación.
«La bioseguridad ya no es una opinión,
es una puntuación:
el nuevo protocolo audita
desde el vallado hasta el carnet de biocidas.»
11. Verificación de limpieza y desinfección tras vaciado sanitario
El procedimiento para considerar válida la limpieza y desinfección es:
- Tomar un mínimo de 2 paños de ≥900 cm² (por cada cara), de varios puntos de la nave.
- Pasar los paños por suelo, paredes, comederos, bebederos, ventiladores, vigas, tuberías, cintas de huevos, cintas de heces, raspadores y puntos difíciles de limpiar.
- Los paños deben humedecerse previamente con diluyentes adecuados (p. ej., NaCl 0,8% + peptona 0,1% en agua desionizada estéril).
- Analizar en laboratorios autorizados dentro de los PNCS.
- Si se detecta Salmonella spp., repetir limpieza y desinfección hasta obtener resultado negativo.
12. Laboratorios
| Tipo | Requisitos |
|---|---|
| Laboratorio Nacional de Referencia | Laboratorio Central de Veterinaria del MAPA (Algete, Madrid) |
| Laboratorios para muestras oficiales | Designados por las CCAA, acreditados EN/ISO 17025, ensayos acreditados para detección de Salmonella en todas las matrices de los PNCS |
| Laboratorios para autocontroles | Reconocidos por las CCAA, mismos requisitos de acreditación EN/ISO 17025 |
Todos los laboratorios deben participar en las pruebas de detección colectivas organizadas por el LNR.
13. Vacunación
- No es obligatoria en reproductoras con carácter general.
- Solo pueden usarse vacunas con autorización de comercialización de la AEMPS o de la Comisión Europea.
- Es obligatoria en reproductoras pesadas cuando se repobla una nave que previamente ha dado positivo: el siguiente lote debe vacunarse antes de la fase de puesta.
- Toda vacunación debe registrarse en el libro de medicamentos y en la aplicación informática del MAPA.
14. Controles oficiales en piensos
- Los operadores de piensos deben disponer de un sistema HACCP documentado.
- Los piensos deben proceder de proveedores registrados o autorizados conforme al Reglamento (CE) 183/2005.
- Cada año se realizan más de 3.000 inspecciones oficiales en establecimientos de alimentación animal y más de 1.000 muestras oficiales de microbiología.
- En productos vegetales: si se detecta Salmonella, se solicita identificación del serotipo; solo si es uno de los 5 serotipos objetivo se notifica a través de la Red de Alerta.
15. Gestión de la carne de manadas positivas a SE/ST en matadero
- El operador debe incluir en la ICA (Información de la Cadena Alimentaria) el resultado del último análisis frente a Salmonella.
- Las manadas positivas a SE/ST se sacrifican mediante sacrificio logístico (último lugar del orden diario), seguido de limpieza y desinfección.
- Los mataderos deben incluir canales de estas manadas en sus planes de muestreo según el Reglamento (CE) 2073/2005.
16. Indemnización a propietarios
- En caso de sacrificio obligatorio, los propietarios tienen derecho a indemnización si han cumplido la normativa vigente.
- Los baremos están recogidos en el RD 823/2010.
- La edad de las aves a efectos de indemnización es la que tenían en el momento en que la autoridad competente ordena el sacrificio.
17. Sistema de monitorización del Programa
- Dos aplicaciones informáticas del MAPA (una para autocontroles, otra para control oficial).
- Doble revisión: las CCAA revisan los datos en su territorio; la Subdirección General realiza la revisión global.
- Plan de control de calidad de autocontroles: los Servicios Veterinarios Oficiales verifican un 5% de las explotaciones en cada CCAA (mínimo 1 granja si hay menos de 20).
- Inspección de laboratorios de autocontrol: cada CCAA debe haber inspeccionado todos los laboratorios de su territorio en un plazo de 2 años.
- Criterios de selección de explotaciones para control de calidad (por orden de prioridad):
- Autocontroles negativos pero control oficial positivo.
- Autocontroles negativos pero comunicación de Salud Pública positiva.
- Autocontroles negativos pero análisis de eficacia LDD positivos.
- Selección aleatoria entre explotaciones sin controles oficiales.
18. Evolución de la prevalencia (2007-2024)
| Año | Prevalencia (% manadas adultas positivas a serotipos objetivo) |
|---|---|
| 2007 (control oficial) | 2,30% |
| 2008 (control oficial) | 2,50% |
| 2009 | 3,30% |
| 2010 | 0,72% |
| 2011 | 0,32% |
| 2012 | 0,12% |
| 2013 | 0,39% |
| 2014 | 0,52% |
| 2015 | 0,28% |
| 2016 | 0,43% |
| 2017 | 0,65% |
| 2018 | 0,52% |
| 2019 | 0,41% |
| 2020 | 0,77% |
| 2021 | 0,12% |
| 2022 | 0,36% |
| 2023 | 0,89% |
| 2024 | 0,78% |
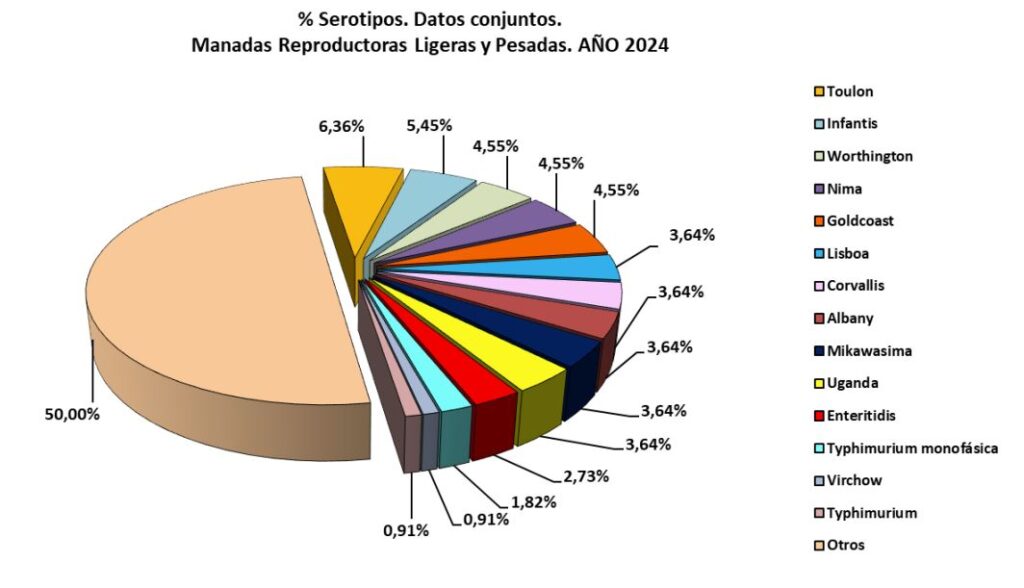
En 2024, los serotipos más prevalentes fueron, por orden: S. Infantis, S. Enteritidis, S. Typhimurium monofásica, S. Typhimurium y S. Virchow.
19. Protección animal durante el vaciado sanitario
Los vaciados sanitarios deben cumplir el Reglamento (CE) 1099/2009 sobre protección de los animales en el momento de la matanza. Las Comunidades Autónomas aplican el documento complementario de protección animal en vaciados sanitarios publicado por el MAPA.
Listado de vacunas contra Salmonella autorizadas en España (actualizado junio 2025)
Disclaimer / Aviso importante:
Este resumen ha sido elaborado por NeXusAvicultura.com a partir del documento oficial «Programa Nacional de Control de Determinados Serotipos de Salmonella en GALLINAS REPRODUCTORAS de la Especie Gallus gallus 2025-2027, Versión 2026«, publicado por la Subdirección General de Sanidad e Higiene Animal y Trazabilidad del Ministerio de Agricultura, Pesca y Alimentación (MAPA).
Tiene carácter informativo y no sustituye al texto legal que puede consultarse completo (46 páginas) en la web del MAPA.
Para saber más:
-. La Salmonella en avicultura
-. Normativa básica y generalidades de los Programas de Control de Salmonela
-. Página principal de Control de Salmonella en avicultura del MAPA
¿Quieres ir un paso por delante en avicultura?
Suscríbete gratis a nuestro eNewsletter y recibe una selección semanal
de la mejor información para anticipar tendencias , estar a la última y mejorar como profesional de la avicultura.
NeXusAvicultura : Visión, Criterio, Calidad y Contexto.


