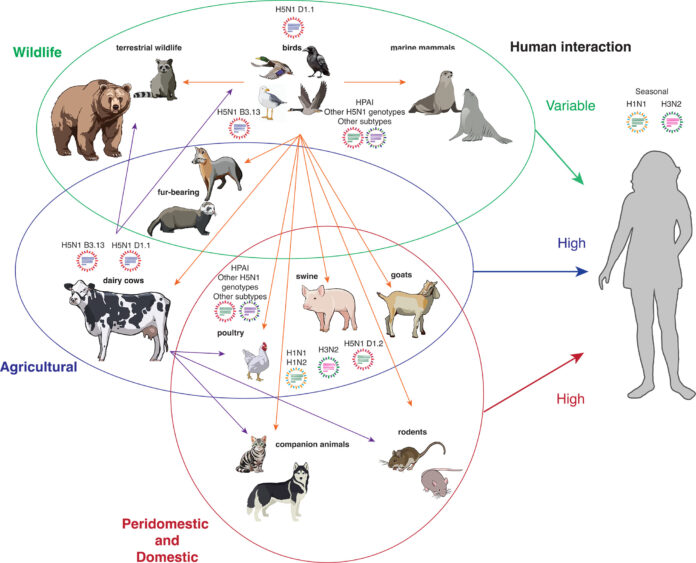
De nueva cepa a panzootia global
El subtipo H5N1 se describió por primera vez en 1966. Aunque entonces ya se sabía que algunas variantes poseían un sitio de clivaje polibásico —clave de su alta patogenicidad en aves—, no fue hasta 1997 cuando se confirmó su capacidad zoonótica tras 18 infecciones humanas en Hong Kong (6 fatalidades). Desde 2021, una ola panzootia impulsada por el clado 2.3.4.4b ha devastado la avicultura mundial y causado mortalidad masiva en aves silvestres y domésticas.
Actualización sobre la situación de la influenza aviar hasta marzo 2025 inclusive
Clado 2.3.4.4b: la evolución que cambió las reglas
- Reasortantes H5NX: desde 2014 surgieron combinaciones H5N2, H5N5, H5N6 y H5N8.
- Expansión global: la variante H5N1 de este clado, originada en Europa en 2021, alcanzó Asia, África y América del Norte vía aves migratorias.
- Neuraminidasa de tallo largo: a diferencia de la NA truncada clásica, este rasgo puede aumentar la aptitud en mamíferos y facilitar saltos de especie.
- Afectación multiespecie: además de aves, se han documentado infecciones y mortalidad en carnívoros domésticos y silvestres, e incluso transmisión mamífero-mamífero en granjas peleteras de España y Finlandia.
Epizootia en bovinos lecheros de EE. UU.
En marzo de 2024 se detectó por sorpresa el genotipo B3.13 en vacas lecheras de Texas. El virus —introducido por un único evento ave-bovino a finales de 2023— se diseminó con rapidez: 973 hatos afectados en 17 estados al 22 de febrero de 2025.
- Vía principal: leche y equipo de ordeño; la leche de vacas infectadas contiene 7-9 log10 TCID₅₀ /ml.
- Clínica: mastitis, caída drástica de producción y secuelas permanentes en animales infectados por vía intramamaria.
- Salud pública: 41 casos confirmados en operarios y evidencia serológica de infecciones subclínicas; 70 casos humanos totales en EE. UU. (22 feb 2025). La mayoría cursan leves, pero existen casos graves y mortales ligados al genotipo D1.1 (procedente de aves, no de bovinos).
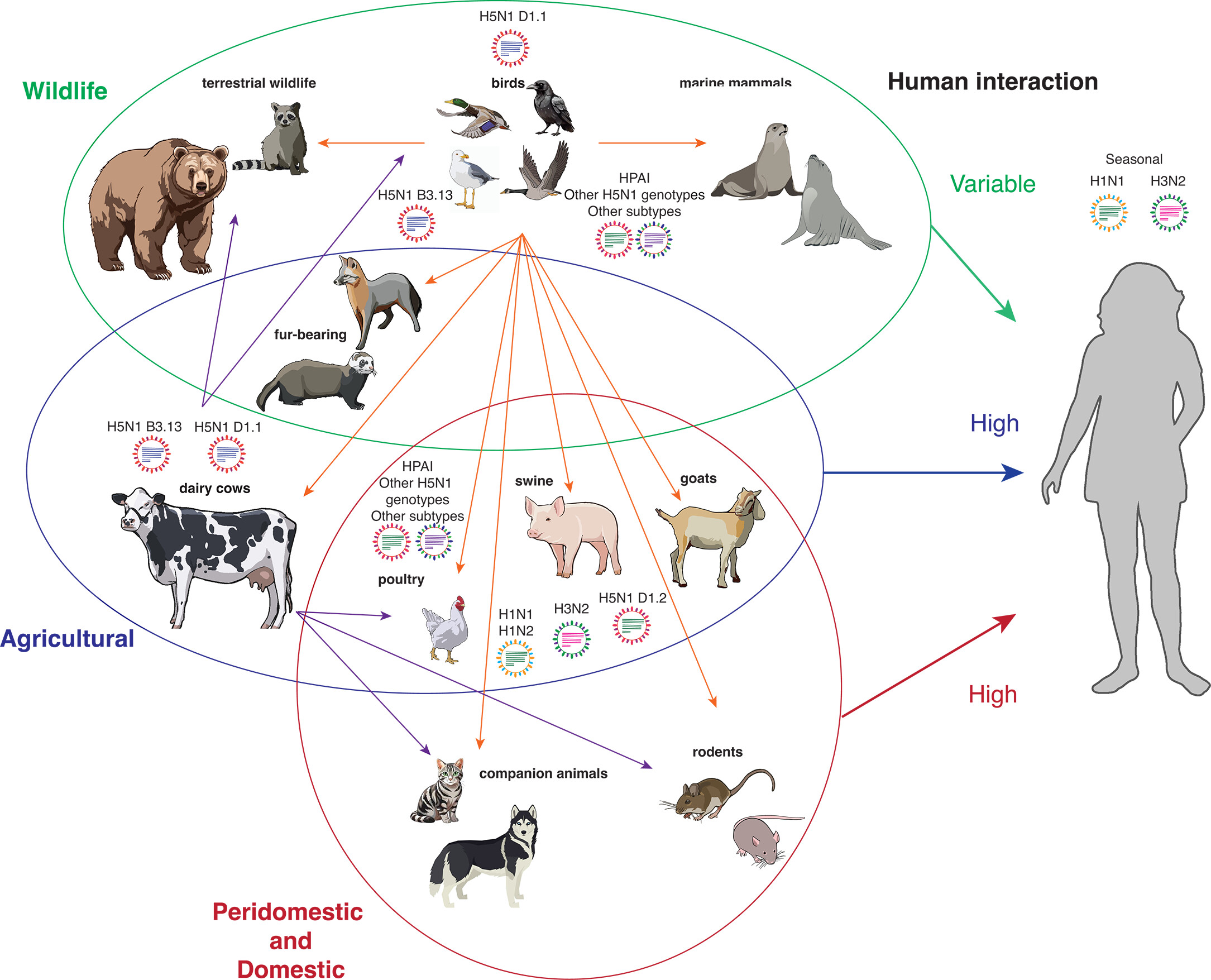
Impacto y riesgos para la avicultura
- Reservorio silvestre: patos migratorios tolerantes facilitan la diseminación y siembran brotes explosivos en granjas de pollos.
- Compatibilidad receptorial en cerdos: la coexpresión de receptores α2,3 y α2,6 convierte a los porcinos en un “reactor de mezcla” potencial para reasortantes con virus estacionales humanos.
- Letalidad humana histórica: 52 % entre 2003-2023 (878 casos, 458 muertes). En la ola actual la tasa aparente es menor, pero la frecuencia de infecciones aumenta y cada nuevo caso amplía la oportunidad de adaptación viral.
Contramedidas disponibles
- Vacunas: existen virus candidatos y una formulación licenciada (A/Astrakhan/3212/2020, H5N8-MF59) que coincide en HA con el clado 2.3.4.4b. Diversos países europeos ya la ofrecen a trabajadores de alto riesgo.
- Antivirales: inhibidores de neuraminidasa y de “cap-snatching” (polimerasa PA) han mostrado eficacia en modelos animales contra estos genotipos.
- Bioseguridad: vacunación de aves y bovinos, control del movimiento de animales, equipos y personas, y refuerzo de EPP para operarios son urgentes para reducir la interfaz ave-humano-mamífero.
El creciente número de especies hospedadoras confirmadas, silvestres y ganaderas, refuerza la necesidad de revisar las medidas de bioseguridad y supervisar la estricta aplicación de las mismas.
El clado 2.3.4.4b H5N1 combina amplio espectro de hospedadores, rápida evolución y capacidad de reasortación. La epizootia bovina revela su potencial para establecerse en nuevas especies productivas, aumentando el riesgo de exposición humana y de aparición de variantes pandémicas.
Para veterinarios de campo y productores avícolas, las prioridades son:
- Vigilancia clínica y virológica continua en aves domésticas y fauna local.
- Refuerzo inmediato de medidas de bioseguridad en explotaciones avícolas y cualquier instalación con interacción interespecies.
- Planificación vacunacional: evaluar la incorporación de antígenos H5 en programas de prevención donde aún no se aplican.
- Formación del personal para reconocer signos tempranos y manejar correctamente equipos y residuos.
La historia demuestra que el virus H5N1 no ha necesitado lograr transmisión sostenida entre humanos para causar pérdidas económicas y sanitarias severas. Contener su circulación en aves y otros animales es, hoy, la barrera más eficaz para evitar el siguiente salto evolutivo.
Fuente:
-. Highly pathogenic avian influenza H5N1: history, current situation, and outlook. Krammer F, Hermann E, Rasmussen AL.2025.. Journal of Virology 99:e02209-24. https://doi.org/10.1128/jvi.02209-24
Para saber más:
-. Estado actual de las vacunas contra la Influenza Aviar (H5N1)
-. Vacunación en avicultura contra la influenza aviar
-. La vacunación de los trabajadores en granjas avícolas en NeXusAvicultura.com